 Як визначити катод і анод + опис
Як визначити катод і анод + опис
Серед термінології в сфері електрики зустрічаються такі поняття, як катод і анод. Це може стосуватися джерел живлення, хімії, фізики та гальваніки. Термін може зустрічатися ще й у вакуумній і напівпровідниковій електроніці. Їм можна позначати висновки або навіть контакти пристрою, а ще, яким електричним знаком вони будуть володіти.
У даній статті ви дізнаєтеся про те, що це таке, а ще як визначити катод і анод в діоді, електролізері, у батарейки, де в них плюс, а де мінус.
Гальваніка і електрохімія
У сфері електрохімії є пару основних розділів:
- Елементи гальваніки-виробництво електричної енергії завдяки рахунку хімічної реакції. До подібних елементів можна віднести акумулятори і батарейки. Їх також часто називають хімічним струмовим джерелом.
- Електроліз-вплив на реакцію хімічного типу електричною енергією, іншими словами – за допомогою Джерела живлення запускається певна реакція.
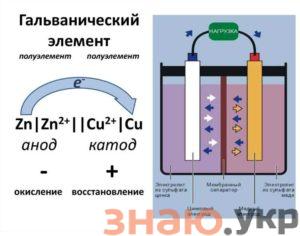
Пропонуємо розглянути окислювально-відновні реакції в Елементах гальванічного типу, і тоді такі процеси відбуваються на його електродах?
 Анод-електрод, і на ньому є окислювальна реакція, а саме він буде віддавати електрони. А ось електрод, на якому буде відбуватися окислювальна реакція називається відновленням.
Анод-електрод, і на ньому є окислювальна реакція, а саме він буде віддавати електрони. А ось електрод, на якому буде відбуватися окислювальна реакція називається відновленням.- Катод-електрод, на якому буде протікати реакція відновлення, а саме він буде приймати електрони. Електрод, на якому буде реакція відновлення – називається окислювачем.
Звідси виникне питання-де мінус, а де плюс у батарейки? Виходячи з визначення, у гальванічних елементів анод буде віддавати електроди.
Зверніть увагу, що в гості 15596-82 дано офіційне формулювання найменувань висновок джерел струму хімічного типу, якщо коротко, то плюс буде тільки на катоді, а мінус на аноді.
В такому випадку буде розглядатися протікання електрики по провіднику зовнішніх ланцюгів від окислювача (тобто катода) до анода, а саме до відновника. Так як електрони в ланцюзі будуть текти від мінуса до плюса, а електрика навпаки, і в такому випадку катод буде плюсом, а анод мінусом. ДО РЕЧІ, струм завжди буде втікати в анод.
Подробиця
Процес електролізу або заряду акумулятора
Такі процеси походи і зворотні гальванічним елементам, так як тут не енергія потрапляє за рахунок реакції хімічного характеру, а навіть навпаки – хімічна реакція буде відбуватися завдяки зовнішньому джерелу електрики. В такому випадку плюсом Джерела живлення все ще будуть називати катодом, а мінус анодом. А ось контакти заряджається елемента гальваніки або електроди електролізера вже здатні носити протилежні найменування, і слід розібратися, чому.
Важливо! При розряді елемента гальваніки елемента анод є мінусом, а катод плюсом, при зарядці все буде навпаки.
Так як струм від позитивного виведення Джерела живлення буде надходити на позитивний висновок акумулятора – Останній до речі вже не зможе бути катодом. Посилаючись на сказане вище, можна зробити висновки, що в такому випадку акумуляторні електроди при зарядці символічно міняють місцями. В такому випадку через електрод заряджається елемента гальваніки, в який втікає струм електрики, називають анодом. Отже, при зарядці плюс акумулятора стане анодом, а мінус буде катодом.
Гальванотехніка
 Процеси металевого осадження в результаті реакції хімічного типу під дією електричного струму (при процесі електролізу) називають гальванотехнікою. Виходить, що світ почав отримувати золочені, посріблені, хромовані або навіть покриті іншими металами прикраси, а ще деталі. Такий процес застосовують в ролі декоративних, а ще в прикладних цілях – для того, щоб покращувати стійкість до корозії різних вузлів і механізмів агрегатів. Метод роботи дії установок для нанесення покриття гальванічного типу буде лежати в застосуванні розчинів солей елементів, якими стануть покривати деталь, в ролі електроліту.
Процеси металевого осадження в результаті реакції хімічного типу під дією електричного струму (при процесі електролізу) називають гальванотехнікою. Виходить, що світ почав отримувати золочені, посріблені, хромовані або навіть покриті іншими металами прикраси, а ще деталі. Такий процес застосовують в ролі декоративних, а ще в прикладних цілях – для того, щоб покращувати стійкість до корозії різних вузлів і механізмів агрегатів. Метод роботи дії установок для нанесення покриття гальванічного типу буде лежати в застосуванні розчинів солей елементів, якими стануть покривати деталь, в ролі електроліту.
Визначити, де анод, а де катод в гальваніці теж важливо. Саме в цьому випадку анод буде електродом, до якого підключаються позитивний висновок Джерела живлення, а виходить, катод в такому випадку стане мінусом. При цьому метал буде осідати (відновлюватися) на мінусовому електроді (мова йде про реакцію відновлення). Виходить, що є ви бажаєте виготовити позолочене кільце власноруч – підключіть до нього негативний висновок блочка харчування і помістіть в ємність з необхідним розчинником.
В електроніці
Ніжки або електроди напівпровідникових, а ще вакуумних електронних пристроїв вкрай часто називають катодом і анодом. Пропонуємо розглянути умовне позначення графічного типу напівпровідникового діода за схемою. Як бачите, анод у діода підключають до плюса батареї. Він так називається з тієї причини-в такий висновок у діода в будь-якому випадку буде втікати струм. На справжньому елементі на катоді буде маркування у воді точки або смужки. Зі світлодіодом все аналогічно, і на 0.5 см світлодіодах нутрощі видно через колбу. Та половина, що більше є катодом. Аналогічним чином буде ситуація навіть з тиристором, призначення висновок і однополярне використання таких триногих компонентів робить його керованим діодом.
У діода вакуумного типу анод теж зазвичай підключається до плюса, а катод до мінуса, як зображена на схемі. Хоча при додатку напруги зворотного типу – назви елементів не поміняються, незважаючи на протікання електричного струму в зворотному напрямку, нехай навіть і незначного. З пасивними елементами, а саме конденсатори і резистори, справи будуть йти інакше. У резистора не буде виділяти окремо аноди і катоди, струм в ньому може почати протікати в будь-якому напрямку. Ви зможете давати будь-які назву для його висновків, і все залежить від ситуації, а також розглянутої схеми. У простих неполярних конденсаторів все точно також. Рідше подібний поділ за найменуваннями контактів буде спостерігатися в електролітичних конденсаторах.
Укладення
Отже, важливо підвести підсумки, відповідаючи на питання – як запам’ятати, де плюс, а де ж мінус у анода і катода? Є зручне мнемонічне правило для електролізу, акумуляторного заряду, гальваніки і приладів напівпровідникового типу. У таких слів з аналогічними найменуваннями однакова кількість букв, що показано нижче. У всіх випадках, які перераховані вище, струм буде витікати з катода, а втікати буде в анод. Нехай вас не збиває з пантелику постійна плутанина ” чому, коли у акумулятора при заряді катод стає негативним, а при звичайних обставинах він позитивний?». Слід пам’ятати про те, що у всіх елементів електроніки, а ще гальваніки і електрозирів – в загальному у вас енергетичних споживачів анодом можна називати висновок, який підключають до плюса. На цьому відмінності закінчаться, і тепер вам буде простіше розбиратися що мінус, що плюс між висновками пристроїв і елементів. Наостанок слід подивитися корисні відеоролику по темі статті. Тепер ви точно знаєте, що таке катод і анод, а ще запам’ятати їх досить швидко. Сподіваємося, ця інформація була для вас цікавою, а ще корисною.
